Trastorn del sistema immunològic
L’EMA demana estar alerta a signes de la síndrome de Guillain-Barré amb AstraZeneca
L’agència europea ja va identificar al maig aquesta afecció durant el procés d’autorització de la llicència condicional de la vacuna
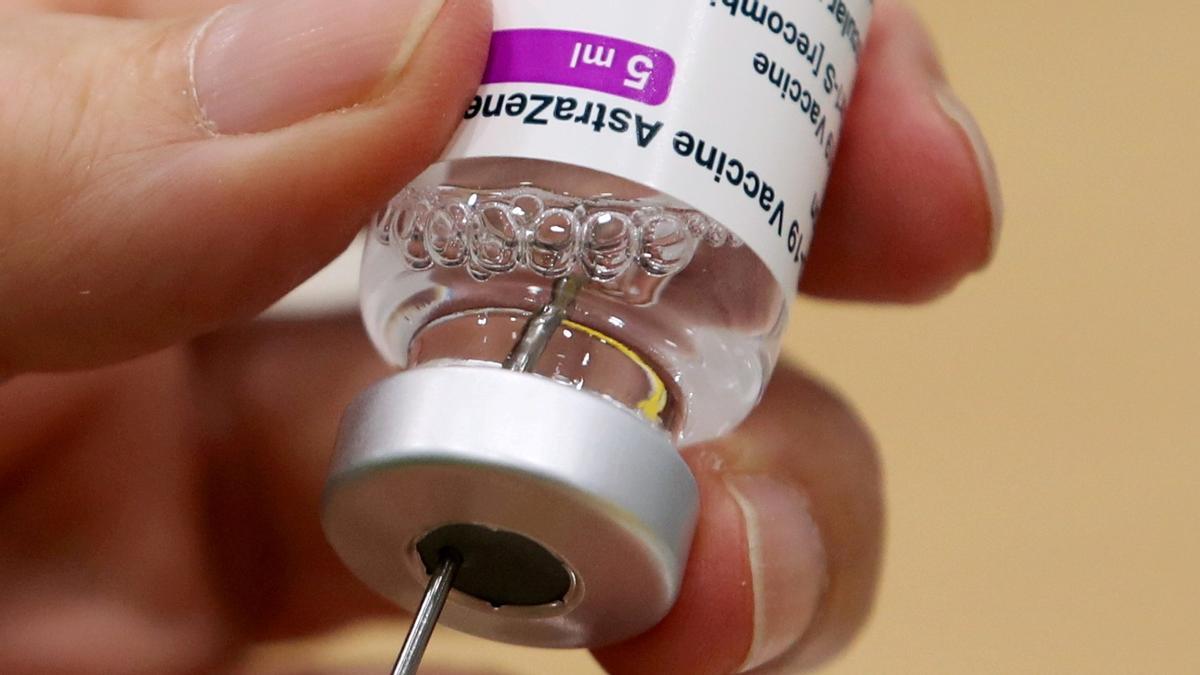
L’Agència Europea de Medicaments (EMA) va remarcar aquest divendres que «no confirma ni descarta de moment» un possible vincle entre la vacuna d’AstraZeneca i la síndrome de Guillain-Barré (GBS, per les seves sigles en anglès), però va advertir els sanitaris i pacients que estiguessin alerta als signes per a un diagnòstic i tractament primerenc.
El comitè de seguretat (PRAC) va recomanar un canvi en la informació del producte d’AstraZeneca (Vaxzevria) per incloure una advertència i conscienciar els professionals sanitaris i les persones que rebin aquesta vacuna sobre els casos de GBS notificats per alguns pacients després de la vacunació.
El PRAC ja ha avaluat tota l’evidència disponible, cosa que inclou informació científica i un número no confirmat de casos notificats a través de la base de dades Eudravigilance per països de l’Espai Econòmic Europeu (EEA), que inclou els 27 de la UE, a més d’Islàndia, Liechtenstein i Noruega.
«Però en aquesta etapa les dades disponibles no confirmen ni descarten una possible associació amb la vacuna», va lamentar.
Una afecció poc freqüent
La síndrome de Guillain-Barré és un trastorn poc comú del sistema immunològic que causa inflamació dels nervis i pot provocar dolor, entumiment, debilitat muscular i dificultat per caminar.
En vista de la gravetat d’aquesta afecció poc freqüent, l’EMA afegirà una advertència de GBS al seu resum de les característiques del producte i al prospecte per a pacients i afegeix que «els professionals de la salut han d’estar alerta als signes i símptomes del GBS, cosa que permet un diagnòstic primerenc, cures i tractament».
Notícies relacionadesEl PRAC aconsella a les persones que reben la vacuna que busquin atenció mèdica «immediata» si desenvolupen «debilitat i paràlisi a les extremitats que poden progressar cap al pit i la cara», tot i que va remarcar que «el balanç benefici-risc de la vacuna es manté sense canvis (positiu)».
L’EMA ja va avisar al maig, quan va iniciar la revisió dels casos notificats, que el GBS es va identificar durant el procés d’autorització de la llicència condicional d’AstraZeneca com «un possible esdeveniment advers que requereix activitats específiques de monitoratge de seguretat», una vigilància que mantindrà més endavant també.
- Espanya arrasa Islàndia i obté el bitllet per al Mundial
- Cine El cinema independent arrela a l'Ebre amb la segona edició de L'Ametlla Film Fest, del 12 al 14 de juny
- Al minut Guerra de l’Iran, en directe: última hora de la situació a l’Orient Mitjà
- Prevost a Barcelona Lleó XIV assegura a l’església de Sant Agustí del Raval que mai va pensar a ser Papa
- Mostra cultural El Cruïlla redobla la seva aposta per ser «molt més que un festival de música»