Assaig clínic mundial
Pfizer i BioNTech avaluen la seva vacuna en embarassades
Es tracta d’un estudi aleatoritzat, controlat amb placebo i cec als observadors en aproximadament 4.000 dones embarassades sanes de 18 anys o més vacunades de la 24a a la 34a setmana de gestació
La farmacèutica espera iniciar investigacions addicionals en nens d’entre 5 i 11 anys «en els pròxims mesos», i en nens menors de 5 anys «més endavant aquest 2021»
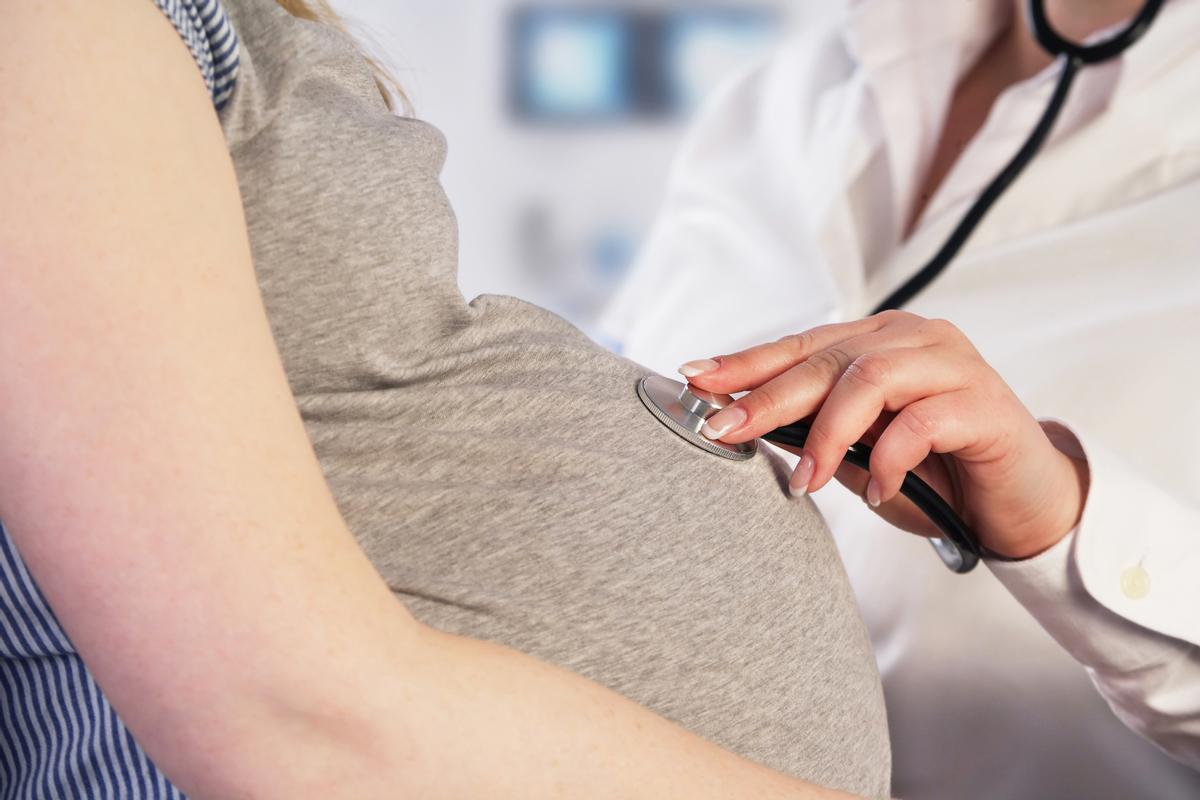
Pfizer i BioNTech han anunciat que s’ha administrat la dosi a les primeres participants en un estudi global de fase 2/3 per continuar avaluant la seguretat, tolerabilitat i immunogenicitat de la seva vacuna contra la Covid-19 en dones embarassades sanes de 18 anys o més.
«Estem orgullosos d’iniciar aquest estudi en dones embarassades i de continuar reunint les proves de seguretat i eficàcia per recolzar potencialment l’ús de la vacuna per part de subpoblacions importants. Les dones embarassades tenen un risc més gran de complicacions i de desenvolupar Covid-19 greu, per això és fonamental que desenvolupem una vacuna que sigui segura i eficaç per a aquesta població. Estem profundament agraïts a les voluntàries que s’estan inscrivint en l’assaig i als investigadors del centre que estan dirigint aquest treball», ha comentat el vicepresident sènior de Recerca i Desenvolupament Clínic de Vacunes de Pfizer, William Gruber.
«Permetre un ampli accés a la nostra vacuna de Covid-19 de gran eficàcia és un objectiu important per a nosaltres. Ara que estem veient l’èxit de la implementació inicial de les campanyes de vacunació a tot el món, és el moment de fer el següent pas i ampliar el nostre programa clínic a altres poblacions vulnerables, com les dones embarassades, per protegir potencialment tant a elles com les generacions futures», ha afegit el director mèdic de BioNTech, Özlem Türeci.
L’assaig de fase 2/3 està dissenyat com un estudi aleatoritzat, controlat amb placebo i cec als observadors en aproximadament 4.000 dones embarassades sanes de 18 anys o més vacunades de la 24a a la 34a setmana de gestació. L’estudi avaluarà la seguretat, tolerabilitat i immunogenicitat de dues dosis de la vacuna o de placebo administrades amb 21 dies de diferència. Cada dona participarà en l’estudi aproximadament durant 7-10 mesos, depenent de si va ser aleatoritzada per rebre la vacuna o el placebo.
L’estudi avaluarà la seguretat en els nadons de les dones embarassades vacunades i la transferència d’anticossos potencialment protectors als fills. Els nadons seran controlats fins aproximadament els sis mesos. Com s’estableix en el protocol de l’estudi, després que neixi el nadó d’una participant, les participants en l’assaig matern seran desemmascarades i les que estaven en el grup de placebo rebran la vacuna.
Notícies relacionadesAbans de portar a terme el seu assaig clínic en dones embarassades, Pfizer i BioNTech van completar una recerca de toxicitat requerit per les autoritats reguladores abans d’iniciar aquesta nova investigació. Aquests estudis no van mostrar cap evidència de toxicitat per a la fertilitat o la reproducció en els animals.
Pfizer i BioNTech esperen iniciar estudis addicionals en nens d’entre 5 i 11 anys «en els pròxims mesos», i en nens menors de 5 anys «més endavant aquest 2021». La seguretat i l’eficàcia en persones de 12 a 15 anys ja s’estan avaluant en un estudi global de fase 3 i està previst presentar-ne les dades pertinents a les autoritats reguladores «en el segon trimestre del 2021». Les companyies també estan planejant estudis per avaluar més la vacuna en persones amb sistemes immunològics compromesos.
- Futbol Sis partits a Prestianni pels insults "homòfobs" a Vinícius
- Motociclisme Àlex Márquez lidera les primeres sessions al circuit de Jerez
- BÀSQUET | EUROLLIGA El viatge d’un Barça decadent es torna a aturar a Mònaco
- El partit de l’Allianz arena El Barça, a la conquesta de Múnic amb la final d’Oslo a l’horitzó
- TENNIS Sinner passa patint a Madrid i Jódar s’exhibeix amb De Miñaur