The Conversation
Això és el que els viròlegs sabem fins avui sobre el coronavirus SARS-CoV-2
zentauroepp52336690 ana200424121237
Albert Bosch, Universitat de Barcelona; Amelia Nieto, Centre Nacional de Biotecnologia (CNB – CSIC); Ana María Doménech Gómez, Universitat Complutense de Madrid; Carlos Briones, Centre d’Astrobiologia (INTA-CSIC); Covadonga Alonso Martí, Institut Nacional d’Investigació i Tecnologia Agrària i Alimentària (INIA); Inmaculada Casas Flecha, Institut de Salut Carles III; Javier Buesa Gómez, Universitat de València; Jesús Navas Castillo, Institut d’Hortofructicultura Subtropical i Mediterrània «La Mayora» ( IHSM – CSIC) (EELM-CSIC) ; José Antonio López Guerrero, Universitat Autònoma de Madrid; Josep Quer Sivila, Hospital Universitari Vall d’Hebrón, Generalitat de Catalunya; Juan E. Echevarría Mayo, Institut de Salut Carles III i Vicente Pallas Benet, Institut de Biologia Molecular i Cel·lular de Plantes (IBMCP – CSIC)
Albert BoschUniversitat de BarcelonaAmelia NietoCentre Nacional de Biotecnologia (CNB – CSIC)Ana María Doménech GómezUniversitat Complutense de MadridCarlos BrionesCentre d’Astrobiologia (INTA-CSIC)Covadonga Alonso MartíInstitut Nacional d’Investigació i Tecnologia Agrària i Alimentària (INIA)Inmaculada Casas FlechaInstitut de Salut Carles IIIJavier Buesa GómezUniversitat de ValènciaJesús Navas CastilloInstitut d’Hortofructicultura Subtropical i Mediterrània «La Mayora» ( IHSM – CSIC) (EELM-CSIC) José Antonio López GuerreroUniversitat Autònoma de MadridJosep Quer SivilaHospital Universitari Vall d’Hebrón, Generalitat de CatalunyaJuan E. Echevarría MayoInstitut de Salut Carles IIIVicente Pallas BenetInstitut de Biologia Molecular i Cel·lular de Plantes (IBMCP – CSIC)Per a Peter Medawar, premi Nobel de medicina el 1960, els virus eren un conjunt de «males notícies embolicades en proteïna». Tot i que no respon a cap criteri científic, aquesta definició reflecteix perfectament la percepció que tenim de la pandèmia del coronavirus SARS-CoV-2 en aquests dies de confinament.
Les «males notícies» en un virus poden venir escrites en dos «alfabets» lleugerament diferents, segons el seu genoma sigui d’ADN o ARN. Els coronavirus (família Coronaviridae) constitueixen un dels grups de virus amb el genoma d’ARN més llarg que es coneix. La informació que conté pot servir per sintetitzar almenys 16 proteïnes.
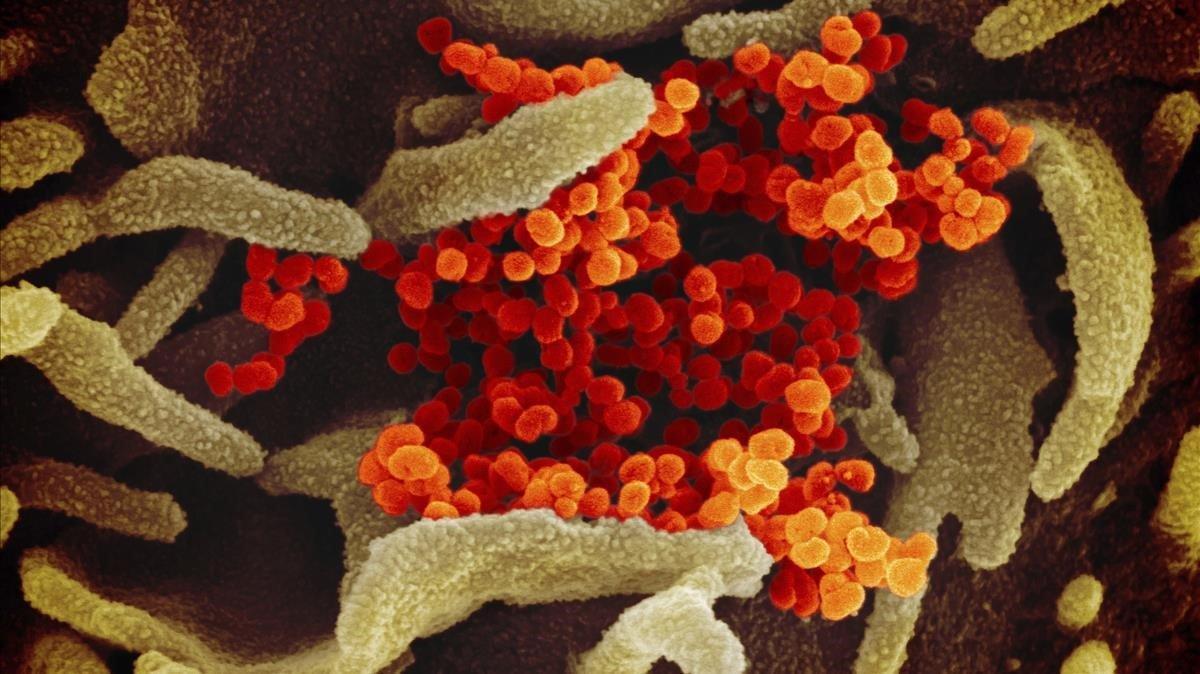
Les més essencials són les que li permeten fer còpies del seu propi genoma, les que protegeixen el seu ARN i les que li permeten entrar a la cèl·lula que infectarà. Aquesta última és una proteïna que conté sucres al seu esquelet i que es projecta a mode d’espícules (proteïna S, de spike, en anglès) des de l’embolcall cap a l’exterior. Al microscopi electrònic creen una imatge que recorda una corona, d’allà el nom del virus.
La fidelitat de còpia de les molècules d’ARN viral és sempre molt menor que les de l’ADN, per la qual cosa els virus d’ARN tendeixen a acumular més mutacions i adaptar-se a nous hostes amb més facilitat que els que tenen un genoma d’ADN. Dins dels virus amb genoma d’ARN, els coronavirus són una excepció: tenen un sistema de correcció de còpia que fa que mostrin una menor variabilitat.
La seqüenciació de més d’11.000 genomes del SARS-CoV-2 ha posat de manifest que té un ritme de mutació 1.000 vegades més lent que el de la grip o el VIH. D’altra banda, els virus amb genoma d’ADN són generalment més difícils d’eliminar perquè alguns d’ells poden produir infeccions latents o fins i tot integrar-se al genoma de l’hoste (això últim també passa amb els virus d’ARN de la família dels retrovirus).
Els coronavirus humans es coneixen des de fa molts anys i la majoria d’ells estan relacionats amb refredats o afeccions respiratòries lleus. L’any 2002 va aparèixer a la Xina el coronavirus primer letal per als humans, el SARS-CoV (nom que prové de «síndrome respiratòria aguda severa»), que va infectar al voltant de 8.000 persones i en va causar la mort de 800, cosa que suposa una taxa de mortalitat del 10%.
Va desaparèixer la primavera del 2004 i des d’aleshores no ha causat més problemes.
El segon, el MERS-CoV (anomenat per la «síndrome respiratòria de l’Orient Mitjà»), va aparèixer a l’Aràbia Saudita el 2012 i va causar aproximadament el mateix nombre de morts, tot i que només va infectar 2.400 persones. La seva taxa de mortalitat va ser del 30%, molt alta, però lluny de l’observada per al virus de l’Ebola (50%) i el virus de la ràbia (95%).
Entre els milers de virus que es coneixen, només una petita proporció són patògens en humans. Les cèl·lules no tenen una porta disponible per a l’entrada de la majoria d’aquests microorganismes.
Però aquests diminuts agents infecciosos han evolucionat mitjançant altes taxes de mutació i recombinació per utilitzar alguna proteïna de l’hoste com a via d’entrada a la cèl·lula, on es podran multiplicar i perpetuar: això és al que qualsevol entitat replicativa aspira, i els virus no poden realitzar-ho per si mateixos fora de les cèl·lules que infecten.
Els coronavirus utilitzen les proteïnes S que formen aquestes espícules al seu exterior per unir-se a una proteïna enzimàtica cel·lular anomenada ACE2. Aquest enzim està situat a la superfície de les cèl·lules de les mucoses, pulmons, artèries, cor, ronyó i intestins, i té la funció de regular la pressió sanguínia, però el virus el fa servir com a porta d’entrada al context cel·lular.
Una vegada dins del seu hoste, el virus campa al seu aire perquè porta amb ell la seva pròpia replicasa que li permetrà fer múltiples còpies del seu genoma (fins a 100.000 còpies a cada cèl·lula) i perquè l’alfabet de la informació que porta en el seu ARN és el mateix que utilitzem els humans.
Els ribosomes cel·lulars no són capaços d’identificar aquest ARN com a estrany. Actua com un cavall de Troya utilitzant la maquinària cel·lular i tradueix la informació esmentada en proteïnes del virus. Això provoca una caiguda de les funcions essencials de la cèl·lula.
Un origen animal desconegut
El SARS-CoV-2 és d’origen animal, tot i que en cap espècie s’ha trobat un coronavirus idèntic o gaire similar. Algunes espècies de ratpenats i el pangolí malai, utilitzat com a aliment i en medicina tradicional xinesa, són reservoris de virus bastant semblants, però els ratpenats estaven hibernant a la Xina el desembre del 2019, quan es van detectar els primers casos en humans.
És necessari continuar investigant per identificar les espècies animals involucrades en l’origen de la pandèmia de Covid-19. Els mercats d’animals vius, salvatges i domèstics, a la Xina són molt freqüents i formen part de la tradicional cadena alimentària del país.
Després d’aquesta pandèmia, el govern xinès hauria de regularitzar-los o prohibir-los. De fet, la següent pandèmia de virus potser ja s’estigui començant a forjar en aquests mateixos entorns.
Com detectar el Covid-19
El diagnòstic de la malaltia Covid-19, causada per aquest coronavirus, es duu a terme detectant l’ARN o els antígens (proteïnes) del virus SARS-CoV-2, o bé els anticossos desenvolupats pel pacient després de ser infectat.
En el primer cas, les mostres que s’utilitzen són secrecions respiratòries que poden contenir el virus (exsudat nasofaringi, exsudat nasal, aspirat traqueobronquial, esput), i en aquestes s’identifica la presència de l’ARN viral (mitjançant la seva extracció i amplificació per PCR quantitativa) o de determinats antígens (fent servir sistemes biosensors de diferent tipus).
Per la seva part, els anticossos del pacient infectat s’analitzen en sang, plasma o sèrum. La detecció d’anticossos davant SARS-CoV-2 permet conèixer que els pacients estan infectats (després d’un «període finestra» d’entre cinc i set dies des de l’exposició al virus, que és el fet servir per l’organisme en generar la resposta immune) i també qui ha superat la infecció fins i tot sense patir-ne els símptomes.
El SARS-CoV-2 és particularment contagiós.
Una taxa de letalitat sobreestimada
Els coronavirus es transmeten per aerosols, on poden romandre viables fins a tres hores, i són estables en diverses superfícies: resisteixen quatre hores sobre el coure (monedes), un dia sencer en el cartró i de dos a tres dies en el plàstic o l’acer inoxidable. El coeficient d’infecció R₀ (nombre mitjà de persones a les quals cada infectat encomana) és de prop de 2,5 (similar a la grip, però molt menys que la verola o el xarampió, que presenten un R₀ de 6 i 15 de mitjana) segons s’ha publicat recentment a la revista The Lancet, i per tant la seva progressió és necessàriament exponencial.
L’altre aspecte numèric important per a la progressió de la pandèmia és la seva taxa de letalitat. Per determinar-la de forma fidedigna es requereix realitzar un mostreig molt ampli. Els càlculs actuals partint de les dades disponibles donen una taxa de letalitat del voltant del 7% de mitjana (tot i que varien molt a les diferents franges d’edat: des d’un 0,7% per als menors de 30 anys fins a un 20% per als majors de 80) a Itàlia i Espanya.
Aquesta taxa mitjana està sens dubte sobreestimada. Tal com va dir el matemàtic Andrejs Dunkels, «és fàcil mentir amb estadístiques», tot i que de seguida va afegir que «és difícil dir la veritat sense». Per a un càlcul precís caldria conèixer el nombre real d’infectats, és a dir, fer les anàlisis a tota la cohort (grup que forma part d’un assaig clínic, en aquest cas la totalitat de la població), la qual cosa és pràcticament irrealitzable.
Però si aquesta cohort la tenim confinada en un creuer, per exemple, estem davant de l’experiment perfecte. Això és el que va passar en el Diamond Princess, on després d’un primer positiu es van fer anàlisi als 3.711 passatgers, inclosa la tripulació, i en alguns casos dues vegades. Durant les següents quatre setmanes es van detectar 711 positius, uns 18% dels quals van ser asimptomàtics.
¿Un milió d’infectats?
En un article publicat per investigadors del Centre de Modelatge Matemàtic per a Malalties Infeccioses de Londres, publicat a la revista Eurosurveillance, es va estimar una taxa de letalitat de l’1,1% en el creuer, molt més baixa que el 3,8% estimat per l’Organització Mundial de la Salut (OMS) a escala global. Si les dades de l’esmentat estudi són correctes i extrapolables, es podria estimar que a Espanya el nombre d’infectats sobrepassaria el milió de persones a dia d’avui i això augmentaria les nostres possibilitats d’estar adquirint una immunitat de grup que ens protegeixi per al futur.
Els coronavirus tenen una membrana lipídica que confereix a la partícula una estabilitat relativament baixa, sobretot si se la compara amb la partícula despullada del virus del refredat comú. Això fa que sigui relativament fàcil eliminar-los de les mans mitjançant solucions sabonoses. Per tant, la protecció sembla senzilla: distància social (seguint l’encertada etiqueta #JoEmQuedoACasa) i correcta higiene de mans.
Segons un estudi recent de l’Imperial College de Londres, si no s’haguessin pres les mesures de confinament el nombre de morts podria haver arribat als 40 milions de persones a tot el món. Però les mesures preventives duradores requereixen l’elaboració de vacunes eficaces. Espanya té una llarga tradició d’investigació en virologia reconeguda internacionalment, essencialment concentrada, però no únicament, a Madrid i Barcelona.
Els nostres companys del Centre Nacional de Biotecnologia del CSIC, els Drs. Luis Enjuanes i Mariano Esteban, estan treballant activament per desenvolupar vacunes contra el SARS-CoV-2 amb dos mètodes basats en principis diferents. L’equip d’Enjuanes pretén atenuar el virus eliminant els gens de virulència del SARS-CoV-2, mantenint els gens responsables de la defensa immunitària.
Per la seva banda, el grup de Mariano Estebanutiliza vectors virals per expressar la proteïna S del virus a la superfície del virus de la vacuna de la verola, que obre la porta cel·lular, esperant que desencadeni la resposta immune. Altres estratègies de laboratoris públics i empreses de diversos països centren el seu esforç en l’ús de fragments de l’ARN viral, l’ADN o proteïnes per generar aquesta resposta protectora en l’organisme.
Però en la situació actual, òbviament, més que mètodes preventius es necessiten urgentment els curatius, basats en compostos antivirals que puguin tractar la infecció. En pacients infectats s’estan provant, entre altres antivirals, la (hidroxi)cloroquina, que impediria la ruta d’entrada del virus, el remdesivir, que actuaria sobre la replicasa viral, i l’associació ritonavir/lopinavir que inhibiria la proteasa utilitzada pel virus per expressar la seva informació.
Altres fàrmacs que s’estan administrant als malalts tenen l’objectiu de controlar o modular la resposta exagerada de la defensa immune davant el mateix virus, incloent interferons, corticoesteroides, anticossos monoclonals com tocilizumab davant el receptor de la interleucina IL-6, eculizumab inhibidor de l’activació del complement, etc.
Siguem optimistes, però pacients
Existeixen diversos assajos clínics en curs a escala mundial (alguns amb participació activa d’hospitals del nostre país), però de moment els resultats no són concloents i els casos d’èxit es refereixen a assajos a petita escala, sense validesa estadística.
Hem de ser optimistes, però pacients. En aquestes circumstàncies es tracta d’una investigació sota una gran pressió i basada gairebé exclusivament en el concepte de prova i error amb compostos farmacològicament aprovats i en ocasions utilitzats anteriorment davant altres virus.
En la fase actual de socialització de la por, d’altra banda comprensible, és important estar ben informats i no contribuir a transmetre, a velocitats més ràpides que la del mateix virus, informacions totalment o parcialment falses. Les segones fan encara més mal, perquè introdueixen dades errònies, manipulades i tendenciosos en un context aparentment bé argumentat.
Aquesta pandèmia ens ha de servir perquè definitivament els governs mundials (en especial l’espanyol) s’adonin de la imperiosa necessitat d’invertir en la generació de coneixement, i que la inversió en Ciència, Educació i Sanitat han de ser la base sobre la qual es construeix una societat justa, igualitària i pròspera.
No oblidem que, segons un estudi d’investigadors de l’Escola de Salut Pública de Boston publicat recentment a la revista Science, fins i tot en el cas de l’eliminació aparent de la pandèmia en els pròxims mesos, les estimacions per als períodes postpandèmia preveuen rebrots ocasionals fins al 2024. No ens queda cap altra opció que estar preparats.
La farmacèutica M. Dolores García i el metge Juan García Costa també ha col·laborat en aquest article. Below is The Conversation's page counter tag. Please DO NOT REMOVE.

Fin del código. Si no ve ningún código arriba, por favor, obtenga el nuevo código de la pestaña Avanzado después de hacer clic en el botón de republicar. El contador de páginas no recoge ningún dato personal. Más información: http://theconversation.com/es/republishing-guidelines
Notícies relacionades
Albert Bosch, Catedràtic de Microbiologia. Dept. Genètica, Microbiologia i Estadística, Facultat de Biologia, Universitat de Barcelona; Amelia Nieto, investigadora retirada, Centre Nacional de Biotecnologia (CNB – CSIC); Ana María Doménech Gómez, Directora Departament de Sanitat Animal, Universitat Complutense de Madrid; Carlos Briones, Científic Titular del CSIC i Vocal de la Junta Directiva de la Societat Espanyola de Virologia, Centre d’Astrobiologia (INTA-CSIC); Covadonga Alonso Martí, Professor d’Investigació, Institut Nacional d’Investigació i Tecnologia Agrària i Alimentària (INIA); Inmaculada Casas Flecha, Investigadora del Centre Nacional de Microbiologia, Institut de Salut Carles III; Javier Buesa Gómez, Catedràtic de Microbiologia, Universitat de València; Jesús Navas Castillo, Investigador Científic CSIC. Professor Associat UMA, Institut d’Hortofructicultura Subtropical i Mediterrània «La Mayora» ( IHSM – CSIC) (EELM-CSIC) ; José Antonio López Guerrero, Professor titular de Microbiologia, Universitat Autònoma de Madrid; Josep Quer Sivila, Responsable de Recerca Bàsica del Virus de l’Hepatitis C del Laboratori de Malalties Hepàtiques Vall d’Hebron Institut de Recerca (VHIR), Hospital Universitari Vall d’Hebrón, Generalitat de Catalunya; Juan E. Echevarría Mayo, Investigador científic del Centre Nacional de Microbiologia, Institut de Salut Carles III i Vicente Pallas Benet, Professor d’Investigació CSIC. Virologia Molecular de Plantes, Institut de Biologia Molecular i Cel·lular de Plantes (IBMCP – CSIC)
Aquest article va ser publicat originalment a The Conversation. Llegiu-ne l’original.

