la lluita contra la Covid-19
Oxford i AstraZeneca reprenen els assajos de la seva vacuna contra el coronavirus
Les proves es van interrompre el dia 6 com a mesura de precaució després de detectar un possible cas advers greu
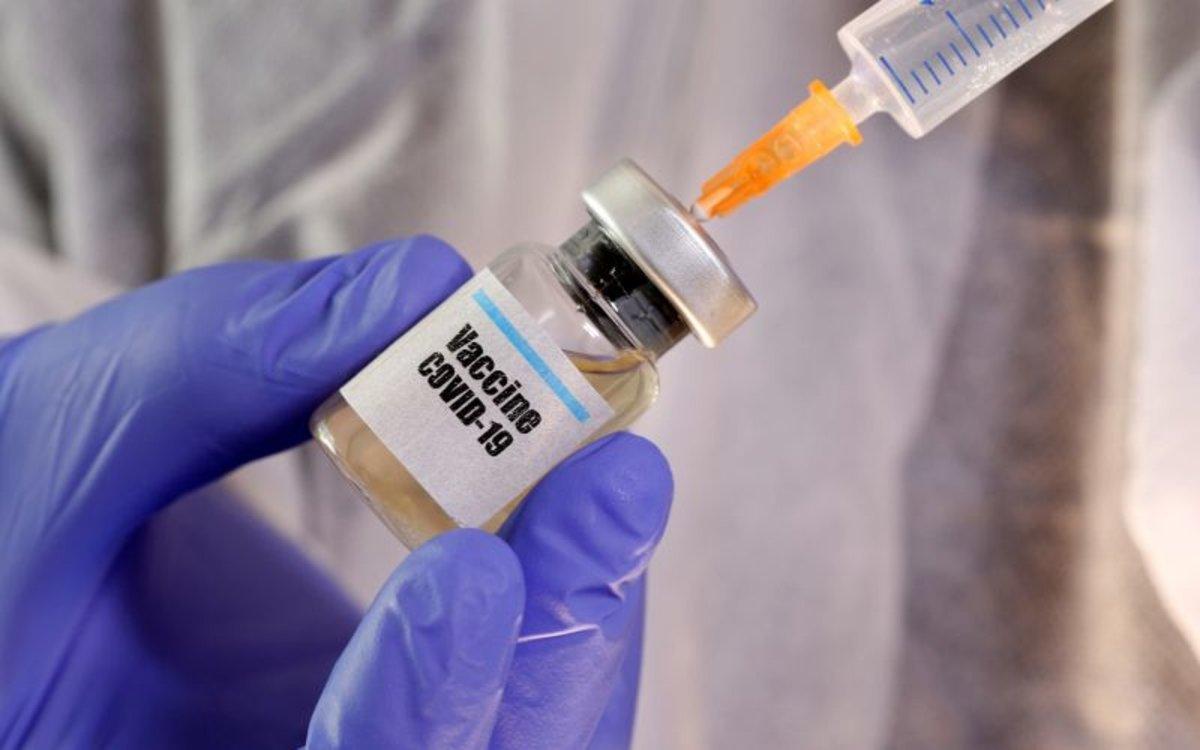
coronavirus-vacuna-reuters
La Universitat d’Oxford i la farmacèutica AstraZeneca reprendran els assajos clínics de la fase 3 de la seva vacuna contra la Covid-19, després de ser recentment interromputs quan un voluntari al Regne Unit va patir una reacció adversa.
En un comunicat, Oxford ha informat que les proves de la vacuna, denominada ChAdOx1 nCoV-19, es reprenen al Regne Unit després de fer una pausa el dia 6 com a mesura de precaució i haver rebut llum verda de les autoritats sanitàries.
«A escala mundial uns 18.000 individus han sigut inoculats amb vacunes experimentals dins del programa de proves», ha apuntat la universitat en un comunicat. «En programes tan amplis com aquest és habitual que alguns dels participants es trobin malament. Cada cas ha de ser avaluat amb cura per garantir una avaluació acurada de la seguretat», explica el text, que no obstant no concreta el dia de represa de les proves.
Una pausa per «malaltia inexplicable»
AstraZeneca va anunciar dimarts que havia decidit interrompre l’assaig de la vacuna que desenvolupa contra la Covid-19 a causa de l’aparició d’«una malaltia potencialment inexplicable» en un dels participants, un moviment que la companyia ha descrit com a «rutinari». «Com a part dels assajos globals controlats i aleatoritzats en curs de la vacuna contra el coronavirus d’Oxford, el nostre procés de revisió estàndard ha interromput la vacunació per permetre la revisió de les dades de seguretat», va indicar la companyia en un comunicat.
«És una acció rutinària que s’ha de fer sempre que hi hagi una malaltia potencialment inexplicable en un dels assajos, així assegurem que manté la integritat», va afegir AstraZeneca.
AstraZeneca té ja contractes subscrits amb el Regne Unit, els Estats Units i la Unió Europea (UE) per al subministrament de dosis de la seva vacuna quan acabi la fase de proves. En concret, la UE ha firmat per comprar 400 dosis de la vacuna, quan la UE a 27 compta amb uns 450 milions d’habitants.
Aquesta possible vacuna, considerada una de les més avançades que es desenvolupen a tot el món, està en les fases finals dels assajos clínics abans de rebre l’autorització dels organismes reguladors per procedir a immunitzar la població.
Notícies relacionadesAls EUA, Pfizer i BioNTech han demanat fer, ja en fase 3, un estudi clínic d’una altra possible vacuna sobre 44.000 participants, que ampliarien els 30.000 inicials amb joves a partir de 16 anys i pacients crònics de sida, hepatitis C i Hepatitis B.
- Procés a Tailàndia La pena de mort s’allunya del cas Daniel Sancho
- El laberint català Així estan les enquestes de les eleccions a Catalunya
- Terratrèmol hores abans de l’inici de la campanya catalana Sánchez anul·la la seva agenda i es planteja renunciar després de la investigació a la seva dona
- BCN expandirà el bus a demanda durant els pròxims tres anys
- A tot Espanya Sanitat no pot cobrir 473 destinacions per a MIR